Usos potenciales de las levaduras marinas de México
Antecedentes
Hace casi 20 años, con el aislamiento de las primeras dos levaduras marinas de la bahía de La Paz en Baja California Sur, México, iniciamos un tema de investigación en microbiología marina en un campo nuevo como una verdadera aventura científica, sin anticipar sus repercusiones. Esos aislamientos, en su momento, fueron seriamente cuestionados en cuanto a su origen, e incluso se consideró que en realidad se trataba de organismos terrestres comerciales utilizados en la elaboración de pan en la ciudad de La Paz, que habían ido a dar al mar a través de las cañerías que entonces descargaban sus efluentes directamente a la bahía (doctor Antonio Peña, comunicación personal). Cuando se realizó el muestreo con el buque oceanográfico El Puma de la Universidad Nacional Autónoma de México (UNAM), en la costa occidental de la Península de Baja California Sur en mayo de 1986, se consiguió el aislamiento de más de 240 organismos levaduriformes (con aspecto de levaduras) en una zona despoblada, sin industria cervecera ni panaderías. La purificación e identificación preliminar de los microorganismos mediante las técnicas convencionales (morfología y pruebas bioquímicas) atrajo el interés de una empresa norteamericana (Nevada Biotech) que aportó el financiamiento necesario para determinar la presencia de la enzima superóxido-dismutasa en los organismos. Su posible aplicación como anti-inflamatorio con fines clínicos fue investigada gracias a los auspicios de La Paz Farmacéuticos, y algunos años más tarde, la compañía Baja ITAL, junto con el Banco Mexicano de Comercio Exterior (Bancomext), proporcionaron el apoyo para la reformulación de un producto cosmético con el objeto de aprovechar las propiedades de la superóxido-dismutasa en la prevención del “envejecimiento”.
Tal vez por estar concentrados en las tareas a las que nos comprometimos con los financiamientos externos, o por ignorancia, la necesidad de asegurar la preservación y viabilidad de las cepas mediante su resiembra periódica (cosa usual en el mantenimiento de un cepario) se consideró de baja prioridad, y al cabo del tiempo sufrimos la irremediable pérdida de 162 cepas. Fue hasta 2001 que la Comisión Nacional para la Biodiversidad, Conabio, vino al rescate para permitir salvaguardar las cepas restantes, comprometiéndonos a establecer la primera Colección de Levaduras Marinas de México a través de un proyecto por encargo.
La importancia en el conocimiento de los microorganismos que habitan en los mares –microbiología marina– se puede enmarcar desde varios puntos de vista: ecológico, biotecnológico y de salud. El primero es importante debido a que la productividad del ecosistema depende en buena medida de las interrelaciones entre los microorganismos. Por otro lado, su presencia o ausencia puede ser indicadora del impacto ambiental asociado a zonas costeras. El segundo aspecto, el biotecnológico, se basa en la preservación y aprovechamiento de estos recursos para la obtención de alimentos, reactivos biológicos y su aplicación en procesos industriales. El tercer argumento para la investigación en microbiología marina descansa sobre la base de que algunos de sus componentes pueden afectar la salud humana.
Las levaduras marinas
Las levaduras son hongos unicelulares de forma ovalada que se reproducen predominantemente por gemación o fisión, dando por resultado un crecimiento unicelular. Algunas pueden ser dimórficas o bifásicas, y crecer como micelio (filamentos) bajo condiciones ambientales apropiadas (Figura 1). Estos microorganismos están incluidos taxonómicamente en la división Eumicota, y dadas sus características de reproducción, se pueden ubicar en tres subdivisiones: Ascomicotina, que comprende a levaduras que pueden formar esporas contenidas dentro de un saco o asca; Basidiomicotina, cuyos representantes forman esporas externas localizadas sobre basidios o esterigmas; y finalmente el grupo Deuteromicotina, que incluye todas aquellas levaduras para las que no ha sido posible demostrar que presentan una fase sexual en su ciclo de vida (Figura 2). La clasificación de las levaduras ha sido confusa y apenas en 1970 se unificaron criterios taxonómicos, identificándose 341 especies; actualmente ya se cuentan más de 500 como miembros del taxón Levaduras (Spencer y Spencer, 1997).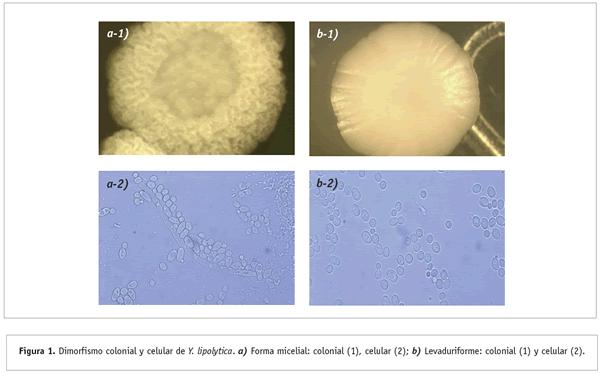
Las levaduras tienen una amplia distribución en variados tipos de hábitat; sin embargo, sabemos mucho menos sobre las levaduras de ambientes acuáticos que sobre las terrestres. Sobre el origen de las levaduras marinas se puede especular que la erosión es uno de los vehículos por el cual los cuerpos de agua (ríos, lagos y regiones marinas costeras) obtienen las levaduras, pero también pueden originarse de la fauna y flora acuática características de este tipo de ambiente, incluyendo el plancton de los océanos. En los últimos 40 años se han reunido evidencias suficientes para establecer que las levaduras que han sido aisladas del ambiente marino son parte constitutiva de la población microbiana marina, por lo que se les puede considerar como “levaduras marinas”. Incluyen a todas aquellas levaduras y organismos levaduriformes que son capaces de constituir y perpetuar poblaciones en el medio marino, o aquellas que se reproducen y crecen preferentemente en el mar, o en condiciones óptimas a las concentraciones normales de sales en el mar, entre 2.4 y 4.0 por ciento de sal de mar (cloruro de sodio). Esta definición no excluye a las levaduras que también son capaces de ocupar, o aun preferir, nichos ecológicos no marinos.
Aplicaciones de las levaduras marinas
Los microorganismos levaduriformes encontrados en el ambiente terrestre han constituido un recurso para la producción a gran escala de antibióticos, enzimas, vitaminas y proteína unicelular. No obstante, muy pocos procesos industriales utilizan organismos marinos, a pesar de que se ha demostrado su potencial como fuente de agentes antivirales, antitumorales, surfactantes (tensoactivos), polímeros, etcétera. El empleo de las levaduras de origen marino en la industria ha quedado rezagado a pesar de que presentan propiedades atractivas, como requerir bajas concentraciones de fuentes de carbono para su crecimiento y desarrollo. El agua de mar, que se puede utilizar en la formulación de los medios de cultivo para el desarrollo de este tipo de organismos, favorece su reproducción en forma selectiva y reduce los riesgos de contaminación que se observan en los procesos que utilizan agua destilada. Las condiciones para el cultivo de Debaryomyces hansenii, cepa de nuestra colección (Figura 2), descrita en varias publicaciones (Ramírez-Orozco y colaboradores, 2001), constituye un ejemplo de las ventajas que pueden alcanzarse en la producción de biomasa con levaduras marinas.
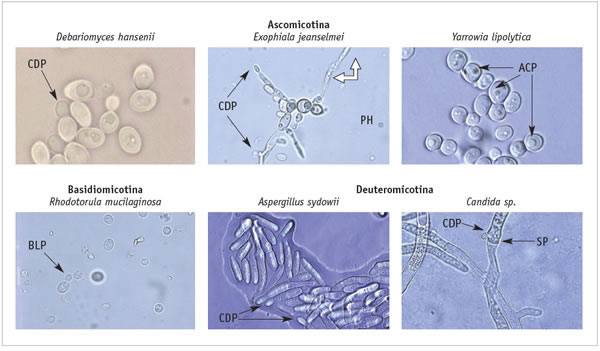
Figura 2. Especies representativas de la Colección de Levaduras Marinas de México del cibnor, pertenecientes a las tres divisiones taxonómicas reconocidas para este grupo de microorganismos. Se indican algunas de las características morfológicas de los grupos: ACP, Ascoespora; BLP, Blastoespora; CDP, Conidioporos; PH, Pseudo-hifa; y SP, Septo.
En ambientes acuáticos, la mayoría de las levaduras probablemente se encuentran creciendo en condiciones sub-óptimas, y para sobrevivir requieren de sitios de reproducción como sedimentos, detritos o asociarse a organismos acuáticos. Del intestino del salmón del Atlántico, por ejemplo, se han aislado diferentes especies de levaduras, siendo dominantes Debaryomyes hansenii, Sacharomyces cerevisiae, Rhodotorula rubra y Rhodotorula glutinis (Andlid, 1995). La adhesividad es tal vez una característica importante para que estas levaduras puedan colonizar y eventualmente incrementar su población en el intestino de los peces. De hecho, se ha propuesto que las levaduras tienen capacidad para cambiar rápidamente las características (fenotipo) de su superficie celular (hidrofóbica-hidrofílica) en respuesta a la disponibilidad de nutrientes, lo que les permite desarrollarse en presencia de los componentes de la mucosa como única fuente de energía y realizar un reconocimiento específico de dichos componentes (Vázquez-Juárez, 1996).
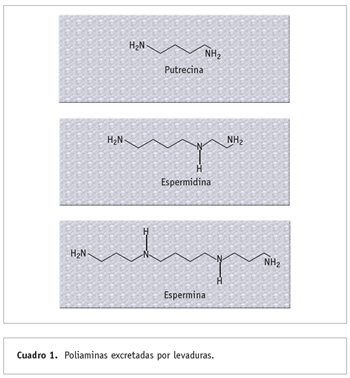
Dos aspectos han motivado la consideración del uso de levaduras como probióticos (benéficos para los seres vivos) en acuacultura: primero, el difundido y probado efecto benéfico de levaduras en diversos modelos, incluyendo al ser humano, y segundo, la demostración de la presencia de levaduras en el tracto digestivo de peces, con una alta capacidad de colonización. Como ejemplo podemos citar a Saccharomyces boulardii, que es ampliamente utilizada en varios países de Europa en el tratamiento de enteritis infecciosa aguda o en los desordenes producidos por el uso de antibióticos (Mcfarland, 1993). Se han descrito diversos mecanismos del efecto benéfico de las levaduras, y entre otras cosas se sugiere que la expresión de enzimas intestinales es favorecida por las poliaminas (Cuadro 1) secretadas por el organismo. En peces, por ejemplo, la diferenciación y maduración del tracto digestivo durante el desarrollo larvario ha recibido especial interés, en respuesta a la creciente demanda de optimizar sistemas de crianza (Tovar, 2002).
 Respecto al uso de levaduras marinas como fuente de la enzima superóxido-dismutasa, podemos comentar que la superóxido-dismutasa de distintos orígenes se ha empleado en medicina como tratamiento para un gran número de desórdenes patológicos de diferentes órganos. Esta enzima también se ha utilizado para controlar los efectos indeseables de la radioterapia (Nelson y colaboradores, 1993) y la quimioterapia (Peskin y colaboradores, 1977), así como en enfermedades inflamatorias (Oyanagui, 1976), reumatismo (Puig-Parellada y Planas, 1978), enfermedades auto-inmunes (Bruroni y colaboradores, 1975) y aterosclerosis (Frazer y Brady, 1978). Considerando el posible uso clínico de la enzima superóxido-dismutasa de cobre y cinc de la levadura marina D. hansenii, hemos realizado diversas pruebas que han permitido poner en evidencia su acción anti-inflamatoria y su eficacia frente a agentes anti-inflamatorios de marca, como el Naproxen, la Dexametasona y el Bristaflam (Cuadro 2). En todos los casos, la superóxido-dismutasa de cobre y cinc de D. hansenii mostró ser superior, lográndose una importante justificación para promover estudios más a fondo sobre su potencial uso biomédico (García-González, 1999).
Respecto al uso de levaduras marinas como fuente de la enzima superóxido-dismutasa, podemos comentar que la superóxido-dismutasa de distintos orígenes se ha empleado en medicina como tratamiento para un gran número de desórdenes patológicos de diferentes órganos. Esta enzima también se ha utilizado para controlar los efectos indeseables de la radioterapia (Nelson y colaboradores, 1993) y la quimioterapia (Peskin y colaboradores, 1977), así como en enfermedades inflamatorias (Oyanagui, 1976), reumatismo (Puig-Parellada y Planas, 1978), enfermedades auto-inmunes (Bruroni y colaboradores, 1975) y aterosclerosis (Frazer y Brady, 1978). Considerando el posible uso clínico de la enzima superóxido-dismutasa de cobre y cinc de la levadura marina D. hansenii, hemos realizado diversas pruebas que han permitido poner en evidencia su acción anti-inflamatoria y su eficacia frente a agentes anti-inflamatorios de marca, como el Naproxen, la Dexametasona y el Bristaflam (Cuadro 2). En todos los casos, la superóxido-dismutasa de cobre y cinc de D. hansenii mostró ser superior, lográndose una importante justificación para promover estudios más a fondo sobre su potencial uso biomédico (García-González, 1999).
Conclusiones
Con la configuración de la Colección de Levaduras Marinas de México (Figura 3), se está dando un paso más en el conocimiento de un componente importante de la microbiota marina de nuestro litoral. La potencialidad de la aplicación biotecnológica de estos organismos está siendo explorada, y la expectativa es llegar a ofrecer nuevos procesos industriales que, empleando agua de mar, permitan la producción de una biomasa unicelular para el desarrollo de nuevos productos.
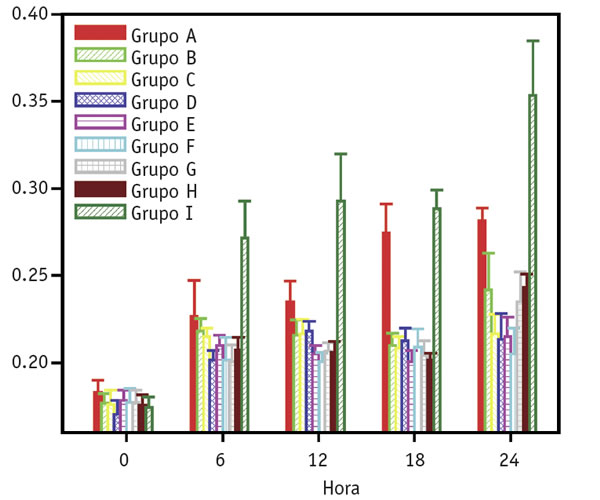
Cuadro 4. Comparación del poder anti-inflamatorio de una crema cosmética (Kiara, Baja Ital, La Paz, Baja California Sur, México) que contiene tepezcohuite, modificada por la adición de la enzima superóxido-dismutasa de cobre y cinc de la levadura marina Debaryomyces hansenii, y un producto comercial (Bristaflam, Aceclofenaco, Bristol-Myers Co.). El modelo experimental utilizado fue el de edema en oreja de ratón. Los grupos estuvieron conformados por tres ratones de aproximadamente 20-25 gramos. La aplicación de las distintas cremas, separadamente, fue externa, 15 minutos después de haber inducido el edema en la oreja derecha del ratón. La oreja izquierda sirvió como control interno. El grupo A estuvo representado por el grupo tratado con la crema cosmética; los grupos B, C y D, recibieron tratamiento con distintas cremas sin antioxidante (methyl parabén) que contenía 5, 10 o 20 microgramos de crema de la enzima; los grupos E, F y G, fueron preparaciones de la crema cosmética con antioxidante y las mismas diferentes proporciones de enzima; el grupo H fue tratado con el producto Bristaflam; finalmente, el grupo I no recibió tratamiento, y por tanto ilustra el grado máximo de edema inducido. El grosor de la oreja (edema) fue medido con un vernier digital. Se puede observar que la inflamación se incrementó con el tiempo (24 horas). El grado máximo de inflamación se observó en el grupo I, como era esperado. En todos los casos, los distintos tratamientos permitieron reducir la inflamación en diferente grado. Las diferencias entre los tratamientos B, C, D, por un lado, y E, F, G, por otro, no fueron estadísticamente significativas, pero sí entre los tratamientos con la crema sin enzima y el producto comercial Bristaflam. Los valores de menor inflamación corresponden a los casos de crema en ausencia de antioxidante. Todo esto permitió concluir que la enzima de la levadura marina posee una acción anti-inflamatoria importante y más efectiva que el Bristaflam.
 |
 |
|
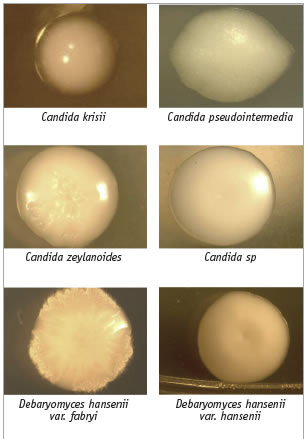
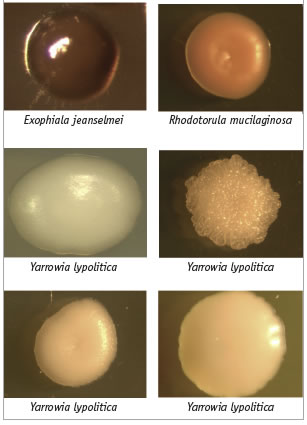
Cuadro 5. Aspecto colonial de algunos ejemplares de la Colección de Levaduras Marinas del cibnor que ilustran no sólo la diversidad de formas, sino también de su aspecto, lo cual sugiere que podrían tener diferentes aplicaciones y usos industriales. |
Bibliografía
Andlid, T. (1995), Ecological physiology of yeasts colonizing the intestine of fish, PhD thesis, University of Goteborg, Sweden.
Bruroni, M., G. Falcioni, E. Fioretti, B. Giarrdina y G. Rotilio (1975), Eur. J. Biochem. 53, 99.
Frazer P. D. y F. O. Brady (1978), Proc. Soc. Exp. Biol. & Med. 159, 30. García González, A. (1999), Tesis.
McFarland, I. V. y P. Bernasconi (1993), “Saccharomyces boulardii: A review of an innovative Biotherapeutic agent”, Microbiol. Ecol. In Health Dis. 6, 157.
Nelson, S. K., S. K. Bose y J. McCord (1994), Free Rad. Biol. Med. 16, 200.
Oyanagui Y. (1976), Biochem. Pharrmacol. 25, 1473.
Peskin A.V., Y. M. Koen y I. B. Zbarsky (1977), FEBS Lett. 78, 41.
Puig-Parellada, P. y J. M. Planas (1978), Biochem. Pharmacol. 27, 535.
Ramírez-Orozco, M., N. Y. Hernández-Saavedra y J. L. Ochoa (2001), Can. J. Microbiol. 47, 676.
Tovar-Ramírez, D. (2002), Comparación de los efectos de la flora digestiva en peces marinos de aguas templadas y tropicales, tesis de doctorado, cibnor, La Paz, Baja California Sur, México.
Vázquez-Juárez, R. (1996), Factors involved in the colonization of fish intestine by yeasts, PhD thesis, University of Goteborg, Sweden.
Jose Luis Ochoa es originario de Chihuahua, Chih., egresado de la Facultad de Química de la unam y doctorado (Ph.D.) del Instituto de Bioquímica de la Universidad de Uppsala, Suecia. Miembro de la amc y de la Sociedad de Bioquímica de México, ha publicado más de 80 trabajos en revistas internacionales y ha sido distinguido con los Premios bcs 2000 y Chihuahua 2002. Es Nivel 3 del sni e Investigador Titular “D” del cibnor.
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
Hever Latisnere Barragán es licenciado en Biología Marina egresado de la Universidad Autónoma de Baja California Sur. Se ha especializado en el uso de herramientas de biología molecular aplicadas a diversas disciplinas científicas a lo largo de cinco años de trabajo. Estas disciplinas van desde aplicaciones en taxonomía molecular hasta análisis de genética de poblaciones en diversos organismos marinos (bacterias y levaduras, hasta crustáceos y elasmobranquios). Ha participado en diversos symposia, cursos y talleres internacionales dentro del tópico molecular y actualmente se desempeña como encargado del laboratorio de Biotecnología de Organismos Marinos del cibnor.
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.

